KUMAMOTO University
R
研究内容RESEARCH CONTENT血液・膠原病・感染症内科学講座では、造血器腫瘍、レトロウイルス感染症を主な研究対象とし、分子生物学、細胞生物学、免疫学、分子ウイルス学的手法を用いて様々な側面から研究を展開しています。以下の研究グループによりプロジェクトを進めていますが、「がん」、「免疫」、「感染症」は各々の病態・進展・治癒機構に深く関わり合っており、グループの垣根を越えた討論により、研究のさらなる発展を目指しています。
成人T細胞白血病(adult T-cell leukemia: ATL)グループ
ATLはヒトT細胞白血病ウイルス1型(human T-cell leukemia virus type 1: HTLV-1)により発症するCD4陽性T細胞の悪性腫瘍である。本研究グループはHTLV-1がATL発がんを惹起する分子機序に関して研究を進めている。HTLV-1感染細胞の生体内での生存、増殖にはHTLV-1プロウイルスのプラス鎖とマイナス鎖に各々コードされるTaxとHTLV-1 bZIP factor(HBZ)が重要な役割を果たす。TaxはHTLV-1の転写を活性化し、ウイルスの複製、個体間伝播に必須である。一方HBZは感染細胞のクローナル増殖に重要な役割を果たすと考えられる。Taxは強力ながんタンパク質であるが、ATL細胞での発現レベルが非常に低いことから、発がんにおける意義は明らかでなかった。我々はこれまでの研究から、Taxはごく一部のATL細胞に一過性に発現することでATLの細胞集団維持に寄与できることを報告した(PNAS, 2018)。一方、HBZは全てのATL症例で発現している。我々が樹立したHBZトランスジェニックマウス(HBZ-Tg)が皮膚炎、肺胞炎といった慢性炎症とTリンパ腫を発症することから(PLOS Pathog, 2011; PNAS, 2020など)、HTLV-1の病原性に必須のウイルス遺伝子であると考えられる。興味深いことに、HBZ遺伝子は翻訳されたタンパク質のみならず、機能的RNAとしても機能している。HBZ RNAはHTLV-1感染細胞では主に核内に存在し、多くの宿主遺伝子の転写を脱制御する(PNAS, 2006; PNAS, 2021)。HBZタンパク質とRNAの作用する分子機序についてさらなる解析を進めている。
ATLグループ

- プレスリリース Press releaese
-
ヒトT細胞白血病ウイルス、エイズウイルスの新しい持続感染メカニズムを発見
https://www.kumamoto-u.ac.jp/whatsnew/seimei/20210513-1 -
日本人に多いヒトT細胞白血病ウイルス1型が炎症とがんを引き起こす新しいメカニズムを解明
https://www.kumamoto-u.ac.jp/whatsnew/seimei/20200601 https://ewww.kumamoto-u.ac.jp/en/news/380/ https://www.eurekalert.org/pub_releases/2020-06/ku-tnm061620.php -
ヒトT細胞白血病ウイルス1型(HTLV-1)の新しい感染維持機構を解明 〜HTLV-1による白血病の発症機序解明と発症予防への応用に期待〜
https://www.kyoto-u.ac.jp/ja/research-news/2018-01-25 https://www.kyoto-u.ac.jp/en/research-news/2018-04-17-0 https://www.eurekalert.org/pub_releases_ml/2018-04/ku-4041118.php
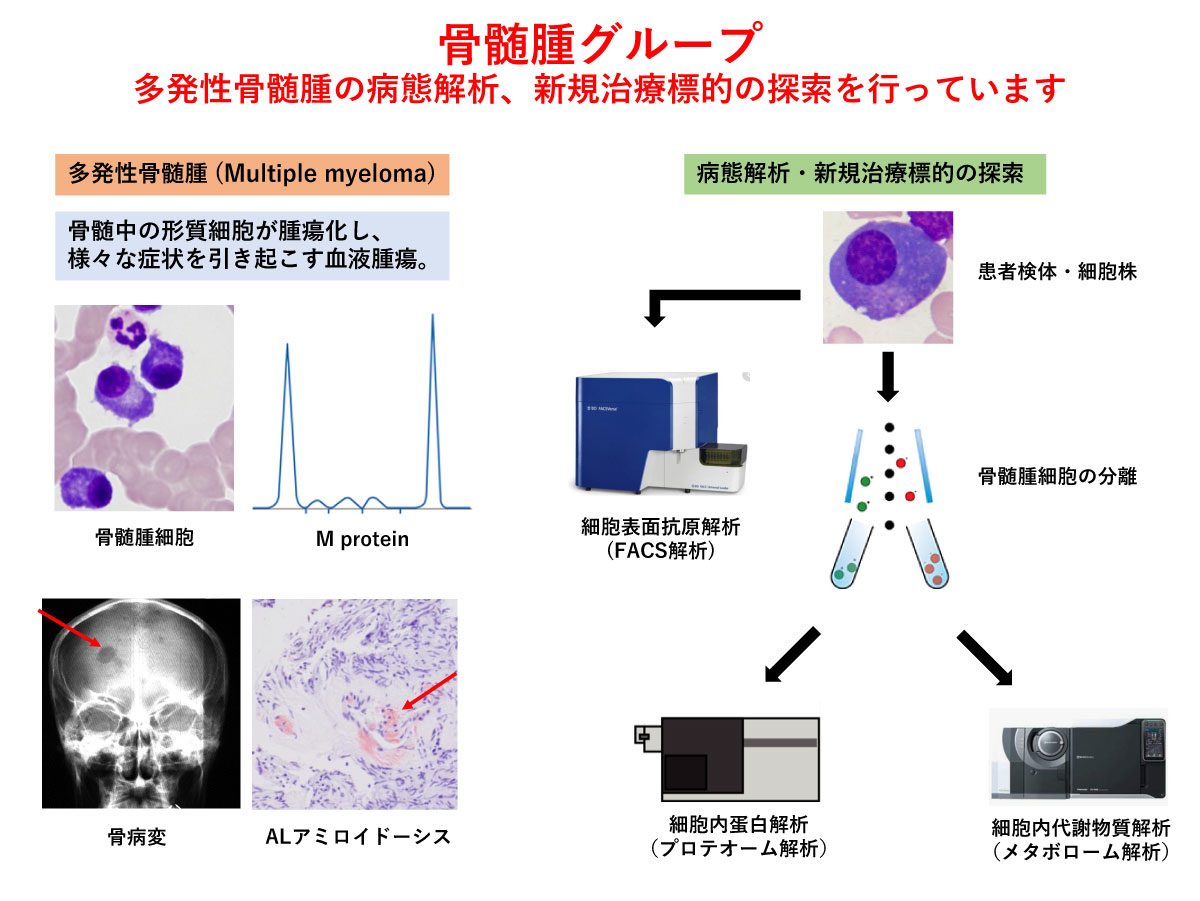
多発性骨髄腫グループ
多発性骨髄腫の病態における骨髄微小環境の役割(J Clin Invest, 2018. Clin Cancer Res, 2018. Leukemia, 2016.)、
骨髄腫細胞の治療標的候補分子(Blood Advances, 2019. Biochem Biophys Res Commun, 2018. Br J Cancer, 2013.)、骨髄腫細胞における表面抗原分子の変化 (Int J Oncol, 2013. Int J Oncol, 2012.)に関する研究結果を報告してきた。
現在、多発性骨髄腫における代謝経路を標的とした治療開発や骨髄腫細胞における表面抗原分子の役割に関する研究を推進している。
骨髄腫 グループ
悪性リンパ腫グループ
悪性リンパ腫発症機序に関する研究を行っている。血球分化に必須の転写因子であるPU.1に着目し、B細胞分化後期にPU.1をノックアウトしたマウスが悪性リンパ腫(DLBCL)を発症することを明らかにした。現在その分子機構について解析を進めている。
白血病グループ
急性白血病の発症には、染色体転座や遺伝子変異などのジェネティックな異常やDNAメチル化やヒストン修飾の変化によるエピジェネティックな異常の蓄積による造血細胞の分化障害が関与している。本グループは臨床検体を用いた解析から分化異常の分子基盤解明を目的とし研究を進めている。
急性骨髄性白血病(acute myeloid leukemia: AML)の亜型として分類されるmyeloid-NK/T細胞の混合表現型白血病はCEBPA遺伝子の発現が抑制されている。我々はCEBPA遺伝子の3’非翻訳領域に存在するエンハンサーがメチル化され発現抑制に関与することを見出した。さらに、この領域にリンパ系転写因子IKZF1が結合することを明らかにし、原著論文として報告した(Eur J Haematol, 2021)。Myeloid-NK/T前駆細胞の起源とその白血化機構に迫る手がかりとなる知見である。
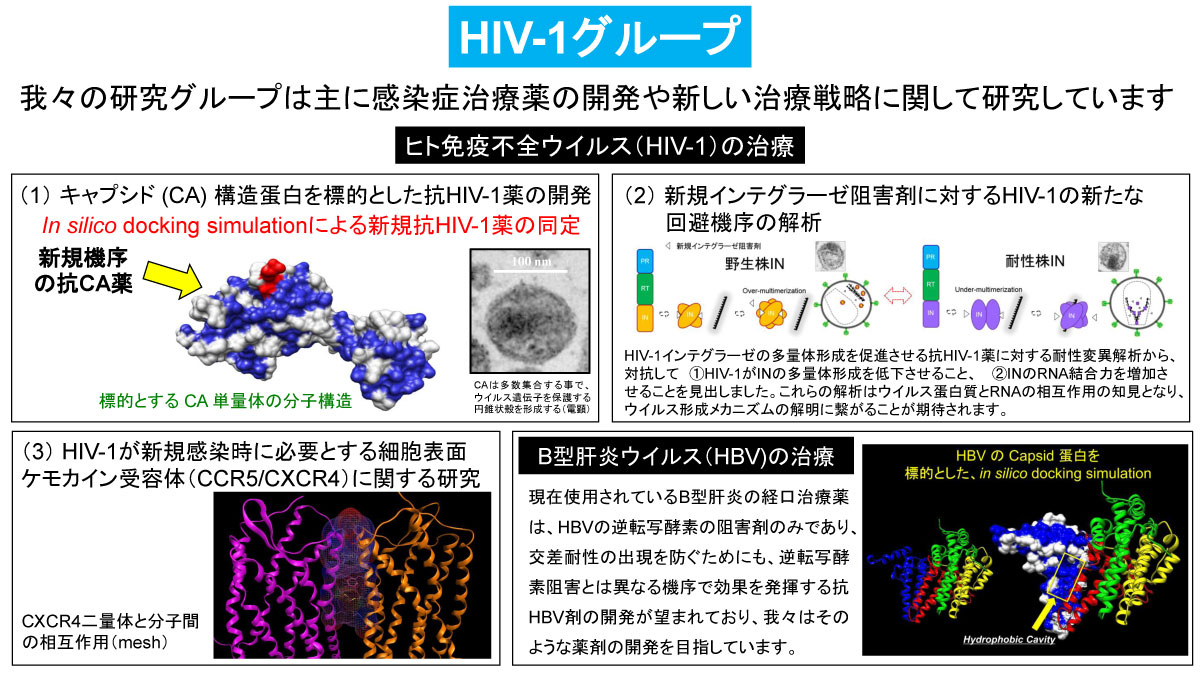
ヒト免疫不全ウイルス(human immunodeficiency virus: HIV)グループ
本研究グループはこれまでに、①新規抗HIV-1化合物の開発;(1) 逆転写酵素阻害剤(AAC, 2007)、(2) CCR5阻害剤(AAC, 2008など)、(3) プロテアーゼ阻害剤(AAC, 2007; Sci Rep, 2017など)、(4) 良好な中枢神経系移行性を有するHIV関連神経認知障害(HAND)治療/予防剤(AAC, 2013; AAC, 2019など)、及び②ウイルス蛋白質の機能解析;(5) アミノ酸挿入変異により起こるキャプシド構造蛋白(CA; HIV-1粒子内でウイルス遺伝子を保護する殻を形成する必須蛋白)の異常な自己崩壊現象の解析(Sci Rep, 2019)、(6) インテグラーゼ阻害剤に対するHIV-1の新たな回避機序の解析(J Virol, 2020)などに関して報告してきた。現在もトランスレーショナルリサーチを継続しており、新規のHIV-1 CA自己崩壊誘導化合物やCA過剰安定化促進化合物を同定開発し、その作用機序の解析等を行っている(投稿準備中)。また、新規抗HBV化合物の開発やHIV-1が新規感染時に必要とする細胞表面ケモカイン受容体(CCR5/CXCR4)に関する研究を並行して行っている。
HIV-1グループ
膠原病グループ
膠原病症例の診療に基づいた臨床研究、臨床検体を用いた解析研究を推進している。
CONTACT US
C
-
患者様へ
外来診療の方は外来予約センターより
ご予約をお願いいたします。
外来予約センター -
学生・研修医・医療関係者の方へ
- TEL
- 096-373-5156
- FAX
- 096-373-5158
- nikyo*kumamoto-u.ac.jp
(*はアットマーク)
